Bewegung im Coulombfeld – Bohr’sche Bahnen
Kreisbahnen im Coulombfeld
Im folgenden betrachten wir die Bewegung eines Elektrons um eine positive
Elementarladung. Dabei beschränken wir uns auf Kreisbahnen.
Im
stationären Fall muss die Summe aus Coulombkraft (Zentripetalkraft) und
Trägheitskraft (Zentrifugalkraft) verschwinden. Für ungleichnamige Ladungen ist
die Coulombkraft negativ.
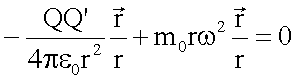
Damit
erhält man in Analogie zum dritten Kepler’schen Gesetz einen Zusammenhang zwischen
Bahnradius und Umlaufzeit (![]() :
:
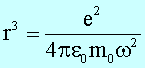
Wir benötigen eine weitere Bedingung, um Bahnradius und Umlaufzeit berechnen zu können. Kennt man den Drehimpuls
![]()
so hat man eine weitere Beziehung zwischen r und w, mit der die gesuchten Größen berechnet werden können. Bei der Beschreibung der Planetenbewegung ist faktisch jeder Wert für L denkbar. Geht man jedoch zu sehr kleinen Beträgen von L über, muss man berücksichtigen, dass der Drehimpuls gequantelt ist. Nach dem zweiten Bohr’schen Postulat genügt der Drehimpuls der Bedingung
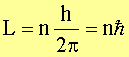
mit h als Planck’schem Wirkungsquantum und n als natürlicher Zahl. Mit n=1 existiert also ein kleinster Drehimpuls.
Mit
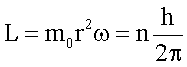
erhält
man
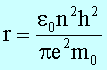
und
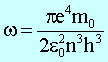
Energiezustände im Coulombfeld
Unter Verwendung der Ausdrücke für r und w können die Energiezustände der Elektronen berechnet werden. Die Gesamtenergie ergibt sich aus der Summe von kinetischer (Rotations-)Energie und potentieller Energie:
![]()
Mit
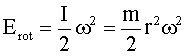
erhält
man
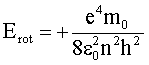
Das Potential einer positiven Elementarladung ist negativ:
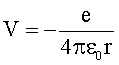
Durch
Einsetzen von r folgt mit ![]()
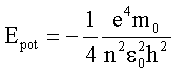
Für die Gesamtenergie folgt somit
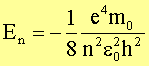
Übergänge zwischen Energiezuständen
Übergänge zwischen verschiedenen Energiezuständen En
(mit n = nA - Anfangszustand und n = nE – Endzustand)
können durch Absorption oder Emission von Lichtquanten der Energie hn und des Drehimpulses h/(2p) erfolgen.
Dabei sind die Sätze von der Erhaltung der Energie und des Drehimpulses
zu beachten:
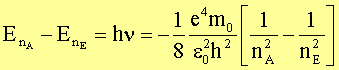
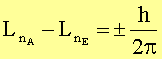 bzw.
bzw. ![]()

Die positiven Vorzeichen für die Energie- und Drehimpulsdifferenzen gelten für Emission von Lichtquanten, die negativen Vorzeichen für Absorption. Damit ist klar, dass die Frequenz der emittierten Lichtquanten n nichts zu tun hat mit der oben berechneten Umlauffrequenz w, wie dies ursprünglich vermutet worden war (siehe Thomson’sches Atommodell).